Պիրոլ
Պիրոլ, հետերոցիկլային միացություն։ Բենզոլի էլեկտրոնային նմանակն է, ունի թույլ արտահայտված արոմատիկ բնույթ։ Պիրոլ անգույն հեղուկ է, հալման ջերմաստիճանը՝ - 23,42 °C, եռմանը՝ 130 °C, խտությունը՝ 969,8 կգ/մ3։
| Պիրոլ | |
|---|---|
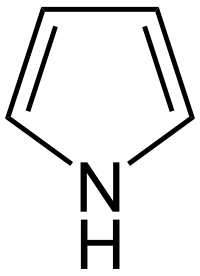 | |
| Քիմիական բանաձև | C₄H₅N |
| Մոլային զանգված | 1,1E−25 կիլոգրամ[1] գ/մոլ |
| Խտություն | 0,9698 գ/սմ³[2] գ/սմ³ |
| Մակերեսային լարվածություն | 38,71 millinewton per metre[3], 37,06 millinewton per metre[3] և 34,31 millinewton per metre[3] Ն/մ |
| Դինամիկ մածուցիկություն | 2,08 միլիպասկալ վայրկյան[4], 1,225 միլիպասկալ վայրկյան[4], 0,828 միլիպասկալ վայրկյան[4] և 0,612 միլիպասկալ վայրկյան[4] Պա/վ |
| Իոնիզացման էներգիա | 1,3E−18 ջոուլ[5] կՋ/մոլ |
| Հալման ջերմաստիճան | −23,39 ± 0,02 °C[2] °C |
| Եռման ջերմաստիճան | 129,74 °C[2] °C |
| Այրման ջերմաստիճան | 39 °C[6][7] |
| Գոլորշու ճնշում | 1,1 kPa[6][7] |
| Քիմիական հատկություններ | |
| pKa | −3,8[8] |
| Բեկման ցուցիչ | 1,5085[2] |
| Դիպոլ մոմենտ | 1,767 ± 0,001 դեբայ[9] |
| Դասակարգում | |
| CAS համար | 109-97-7 |
| PubChem | 8027 |
| EINECS համար | 203-724-7 |
| SMILES | C1=CNC=C1 |
| ЕС | 203-724-7 |
| RTECS | UX9275000 |
| ChEBI | 7736 |
| Եթե հատուկ նշված չէ, ապա բոլոր արժեքները բերված են ստանդարտ պայմանների համար (25 °C, 100 կՊա) | |
Քիմիական հատկություններ
խմբագրելՕդում մգանում է։ Դանդաղ խեժանում է թթուների ազդեցությամբ։ Լավ է լուծվում սպիրտում, եթերում, բենզոլում, սահմանափակ՝ ջրում։ Պիրոլ միջուկը պորֆիրինների հիմնական կառուցվածքային բաղադրիչն է։ Պիրոլ ածանցյալներն են․ հեմինը, քլորոֆիլը, բազմաթիվ ալկալոիդներ (նիկոտին, ատրոպին, կոկաին ևն) և ամինաթթուներ (պրոլին, տրիպտոֆան ևն)։
Ստացում
խմբագրելՀ․ Չամիչյանի հետազոտությունների շնորհիվ Պիրոլի քիմիան օրգանական քիմիայի լավ ուսումնասիրված բաժիններից է։ Հիդրվում է (H2, Ni, 200 °C)՝ առաջացնելով պիրոլիդին, օքսիդանում՝ առաջացնելով մելամինաթթվի իմիդը։ Պիրոլ ստանում են լորձաթթվի ամոնիումային աղի չոր թորումով, նաև ֆուրանի և ամոնիակի խառնուրդից (A1203, 400-450 С)։ Օգտագործում են պիրոլիդին ստանալու, հականեխիչ և մանրէասպան դեղանյութերի (օրինակ՝ յոդոլի) սինթեզի համար։
Ծանոթագրություններ
խմբագրել- ↑ 1,0 1,1 PYRROLE
- ↑ 2,0 2,1 2,2 2,3 2,4 2,5 2,6 CRC Handbook of Chemistry and Physics / W. M. Haynes — 97 — Boca Raton: 2016. — P. 3—478. — ISBN 978-1-4987-5428-6
- ↑ 3,0 3,1 3,2 3,3 3,4 3,5 CRC Handbook of Chemistry and Physics / W. M. Haynes — 97 — Boca Raton: 2016. — P. 6—193. — ISBN 978-1-4987-5428-6
- ↑ 4,0 4,1 4,2 4,3 4,4 4,5 4,6 4,7 CRC Handbook of Chemistry and Physics / W. M. Haynes — 97 — Boca Raton: 2016. — P. 6—246. — ISBN 978-1-4987-5428-6
- ↑ 5,0 5,1 David R. Lide, Jr. Basic laboratory and industrial chemicals: A CRC quick reference handbook — CRC Press, 1993. — ISBN 978-0-8493-4498-5
- ↑ 6,0 6,1 CRC Handbook of Chemistry and Physics / W. M. Haynes — 97 — Boca Raton: 2016. — P. 15—19. — ISBN 978-1-4987-5428-6
- ↑ 7,0 7,1 CRC Handbook of Chemistry and Physics / W. M. Haynes — 97 — Boca Raton: 2016. — P. 16—29. — ISBN 978-1-4987-5428-6
- ↑ CRC Handbook of Chemistry and Physics / W. M. Haynes — 97 — Boca Raton: 2016. — P. 5—96. — ISBN 978-1-4987-5428-6
- ↑ CRC Handbook of Chemistry and Physics / W. M. Haynes — 97 — Boca Raton: 2016. — P. 9—65. — ISBN 978-1-4987-5428-6
| Վիքիպահեստն ունի նյութեր, որոնք վերաբերում են «Պիրոլ» հոդվածին։ |
| Այս հոդվածի կամ նրա բաժնի որոշակի հատվածի սկզբնական կամ ներկայիս տարբերակը վերցված է Քրիեյթիվ Քոմմոնս Նշում–Համանման տարածում 3.0 (Creative Commons BY-SA 3.0) ազատ թույլատրագրով թողարկված Հայկական սովետական հանրագիտարանից (հ․ 9, էջ 309)։ |